酸度和碱度的概念 HORIBA堀场
酸度和碱度的概念
氢离子浓度

水溶液的酸度或碱度由什么决定?
事实上,水溶液的酸度或碱度是由氢离子的浓度决定的,即水溶液中所含氢离子的比例。
我们以普通水为例。
如您所知,水的分子式为H 2 O,但实际上大部分水以非常稳定的分子形式存在,称为H 2 O。
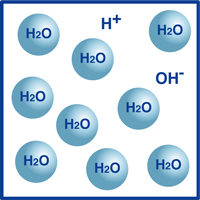
然而,在大气的一小部分中,氢离子H +和氢氧根离子OH -以单独的形式存在。
换句话说,它看起来像右图。
事实上,氢离子和氢氧根离子之间的平衡是决定pH值的元素。
如果氢离子较多,则呈酸性;如果氢氧根离子较多,则呈碱性。
只要温度恒定,任何水溶液中氢离子浓度[H + ]和氢氧根离子浓度[OH- ]之间总是观察到以下关系。
[H + ][OH - ]=Kw=10 -14 (=常数) (水温25℃时)
Kw 称为“水的离子积”或“水的离解常数”。
在纯水或中性溶液中,
由于[H + ]=[OH - ]
[H + ]=[OH - ]=√(Kw)=√10 -14 =10 -7
(√=根)
如果您知道[H + ] 或 [OH - ]的值,您也可以知道另一个的值。
因此,实际上,仅测量[H + ],并将其用作 pH 值的指导。这就是为什么 pH 值是由氢离子浓度决定的。

pH值由以下公式定义:
pH=-log10[H + ]
我们接触到的水溶液的氢离子浓度有时约为每升1摩尔,有时约为每升0.000001摩尔。然而,特别是在需要测量pH值的氢离子浓度非常低的水溶液的情况下,存在大量的小数位,使得数学上处理起来不方便。丹麦化学家Sørensen提出pH值是用常用对数表示的氢离子浓度的倒数。IE。
pH=-log10[H + ]
在溶液为中性的情况下,
由于[H + ]=10 -7 ,因此pH值为7。
由上可知,例如pH 4表示水溶液中氢离子浓度为10 -4 mol/L,即1升水溶液中含有0.0001 mol氢离子。
类似地,pH5含有10 -5 mol/L,pH6含有10 -6 mol/L,pH7含有10 -7 mol/L氢离子。这里您会注意到,尽管在比较 pH4 和 pH7 时氢离子浓度相差 1000 倍,但在显示 pH 时可以简单地表示为 3 个单位的差异。通过这种方式用指数(幂数)来表达大量变化的好处可以从下图看出。
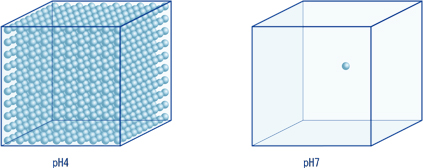
当氢离子为10 -4 mol/L(左)和10 -7 mol/L(右)时,氢离子的数量相差1000倍,但pH值的差异可以表示为3((一个蓝色圆圈代表10 -7 mol/L氢离子)。
*mol/L:化学中用于测量物质含量的单位之一是摩尔。这是阿伏伽德罗的几个粒子(原子、分子、离子)的集合(6.02 x 10 23 个粒子)。浓度单位mol/L表示1升溶液中溶解有多少摩尔物质。

